台灣抗疫捷報!新藥通過美FDA二期臨床試驗
【新唐人亞太台 2020 年 06 月 17 日訊】再來看到台灣對抗疫情的捷報!台灣專門研發小分子藥物的生技公司國鼎,研發出新藥,通過美國FDA二期臨床試驗。業者表示,若二期臨床試驗通過後,不須再經過三期臨床試驗,只要取得美國緊急使用授權(EUA)許可後,最快年今底前就能上市。
國鼎生技董事長 劉勝勇:「台灣第一個進入美國FDA,2期臨床的武漢肺炎的新藥。」
治療武漢(中共)肺炎藥物,再現曙光。由台灣生技公司,針對輕度到中度的武漢肺炎病患,研發出的新藥,通過美國FDA核准,進行安全性和功效性的試驗,也是台灣第一個、美國少數,進入到2期臨床的藥廠。
國鼎生技董事長 劉勝勇:「是因為我們長期10年來,研究這個小分子藥物。我們有非常龐大的資料庫,所以在這一次能夠在1個多月裡面,就完成申請核准。」
國鼎生技總經理 蘇經天:「這次做完了之後,我們就會拿著數據就是跟FDA(美國食品藥物管理局)討論,如果它可以應用EUA(美國緊急使用授權)的方式,讓它可以用,比較快速的審查的方式的上話,那也許年底或是明年初(上市),那應該就會是最好的時間點。」
生技公司表示,這款新藥,屬於單一治療。在細胞與動物實驗中發現,可以降低病毒在細胞內的核酸複製,與病毒蛋白的合成,阻止發炎反應,所造成的器官組織傷害。
國鼎生技總經理 蘇經天:「很多的過去這些病毒它,使用完了之後它都有纖維化的問題,那我們是唯一個就是,三個功能(抗病毒抗發炎抗纖維化),同時都能夠針對這個病。」
國鼎生技董事長 劉勝勇:「台灣的抗疫做得非常好,那未來,如果是有這種需要的狀況,我們還是會台灣優先提供。」
目前治療武漢(中共)肺炎藥物,共有5種,包括瑞德西韋、羥氯奎寧、廣效型抗冠狀病毒抗體、蛋白?抑制劑以及單株抗體藥物。其中,瑞德西韋原本是用在治療伊波拉病毒,目前在全世界進行跨國臨床試驗,台灣有3家醫院參與,5月底獲准食藥署(TFDA)有條件使用,1000人次藥品最快7月底前抵台。
新唐人亞太電視 陳輝模 李晶晶 台灣台北報導
相關新聞
-

台廠抗疫口服新藥解盲成功!拼4月拿到美國EUA
2022-01-05 22:24:42對抗中共病毒,台灣一家生技公司今天公布,口服藥物2期解盲達標,輕中度患者康復率可達百分之百,將向美國食藥署申請緊急使用授權。台灣防疫指揮官陳時中對此抱有期待。
-

中國疫情嚴峻 多地猝死暴增
2024-04-06 19:38:56中國大陸的疫情從未消失。日前,多地民眾反映,從去年底至今,身邊許多人出現染疫重症,猝死率暴增。由於太多人死,大家都不願意去殯儀館,也不開追悼會了。
-

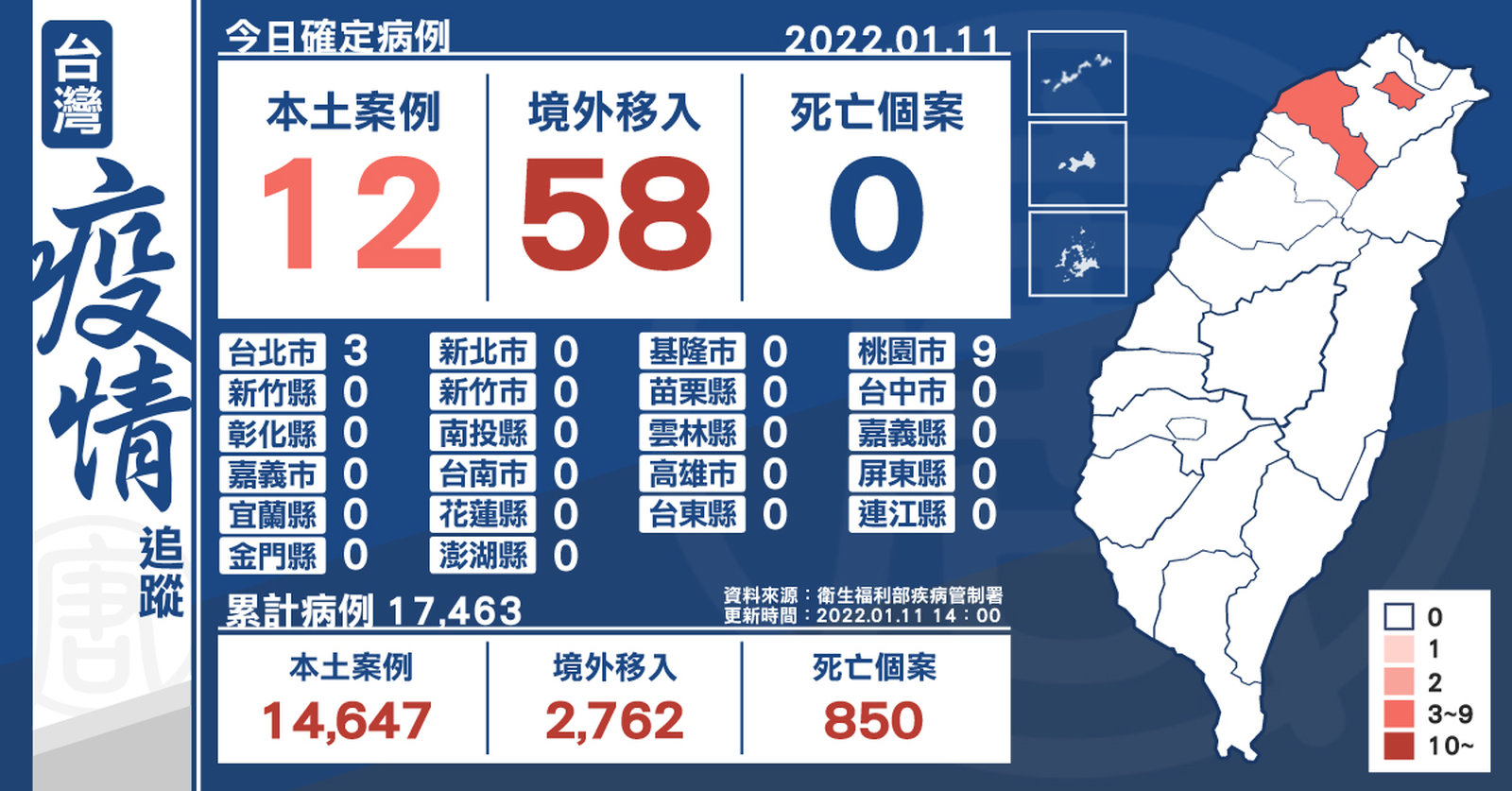
+12例本土 今早落地採陽17例 新增電子工廠群聚下午已停工
2022-01-11 16:07:49今(11)日中央流行疫情指揮中心公布,國內新增12例本土個案及58例境外移入;另確診個案中無新增死亡。
-

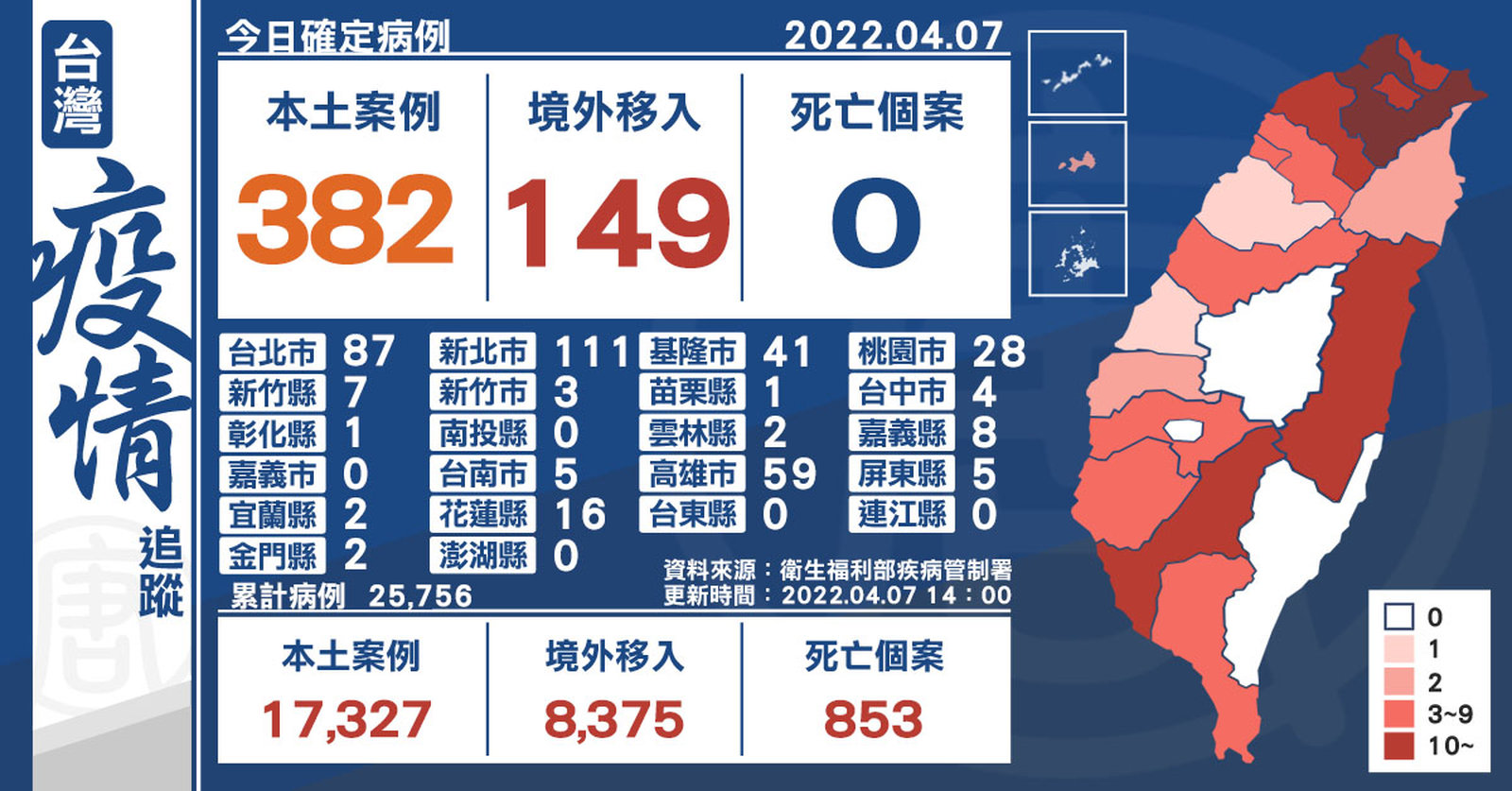
本土+382 金門2例陰轉陽 境外+149
2022-04-07 14:46:21中央流行疫情指揮中心今(7)日公布,國內新增531例COVID-19確定病例,分別為382例本土個案及149例境外移入,其中78例為航班落地採檢陽性;另確診個案無新增死亡。
-

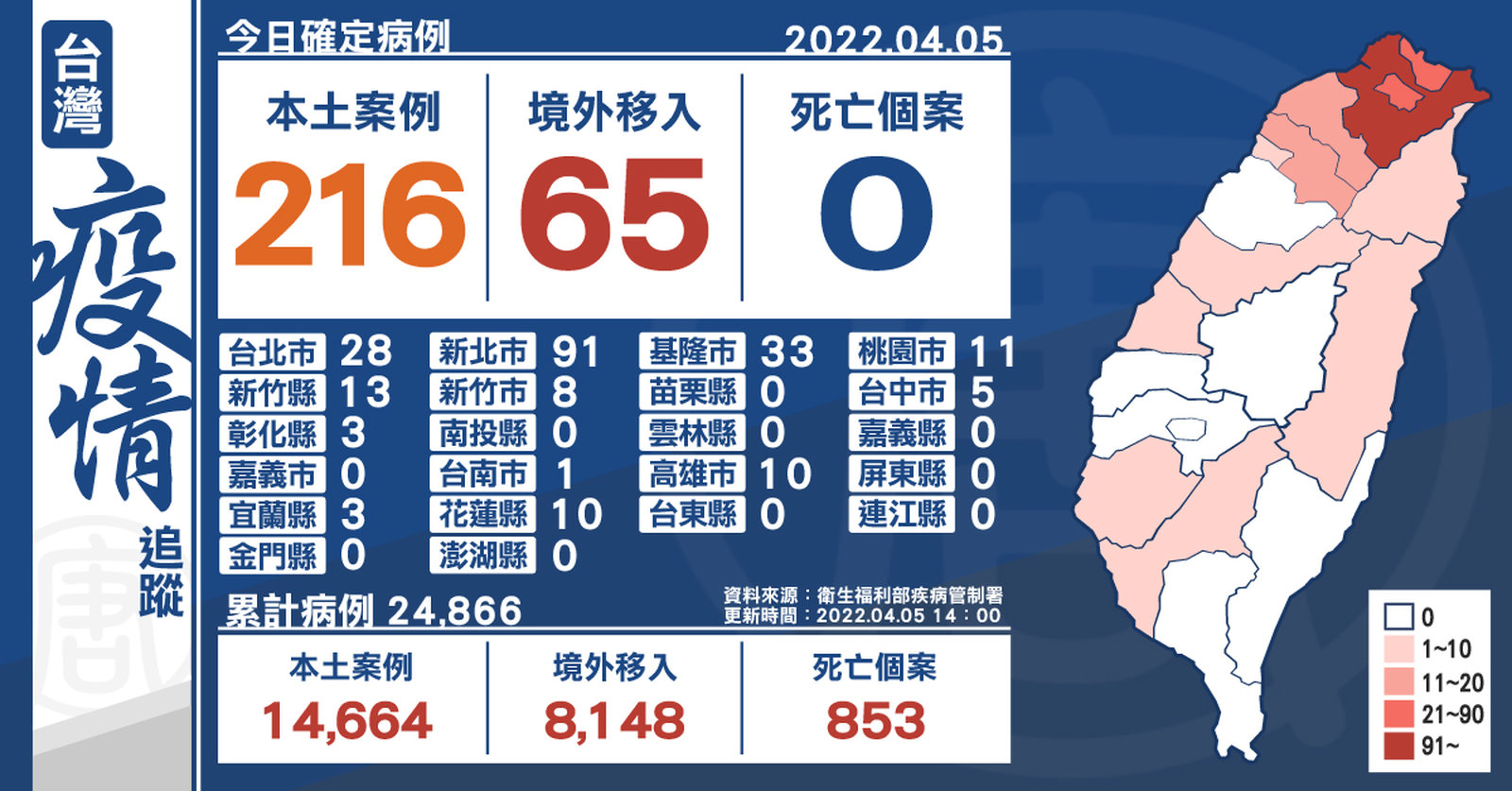
台本土+216今年首破200 新北91、基隆33
2022-04-05 14:31:22中央流行疫情指揮中心今(5)日公布,國內新增281例COVID-19確定病例,分別為216例本土個案及65例境外移入,其中28例為航班落地採檢陽性;另確診個案無新增死亡。
-

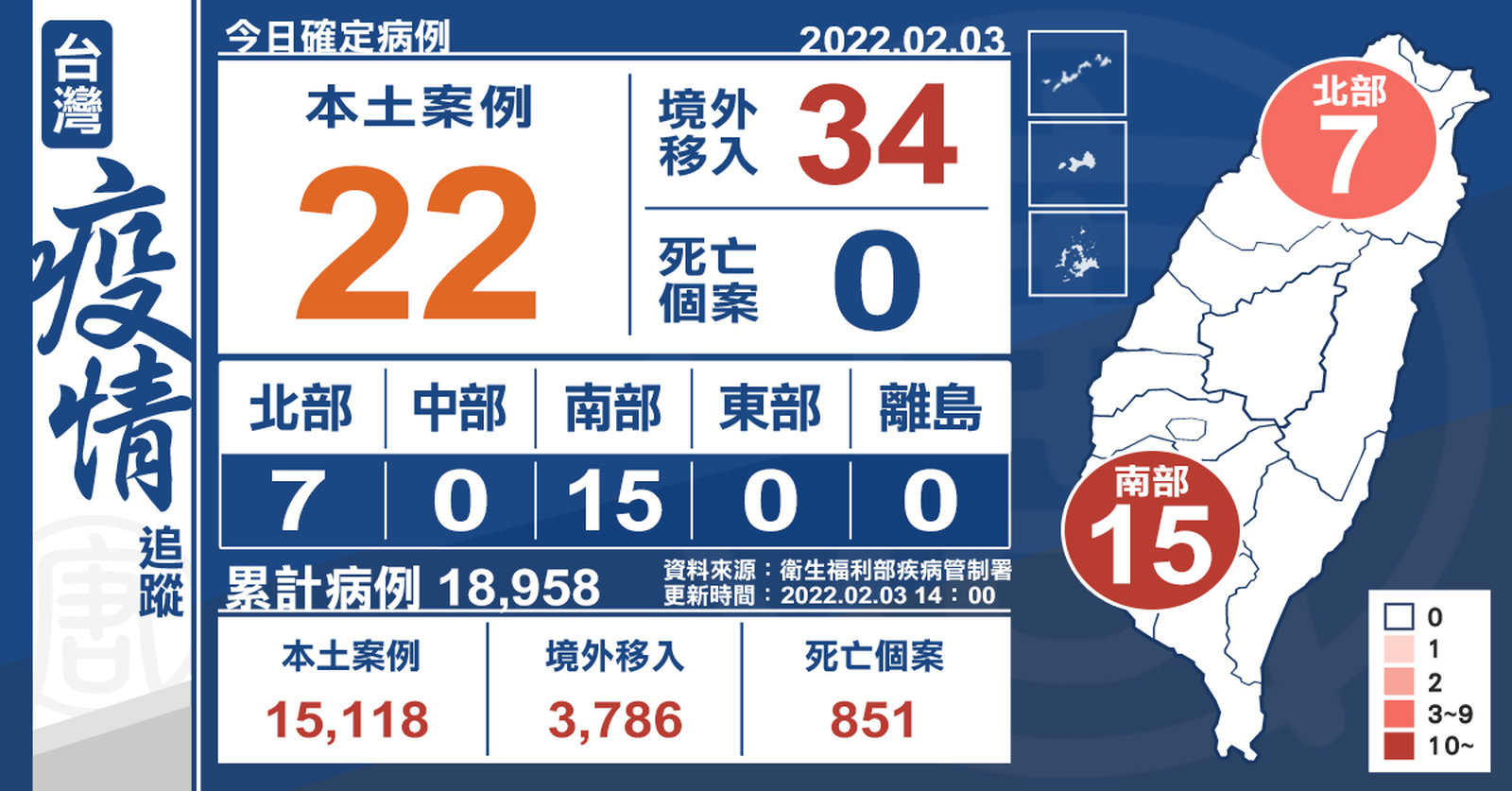
初三本土+22例!中國返台過年1家4口確診
2022-02-04 22:19:14中央流行疫情指揮中心今(3)日公布國內新增56例COVID-19確定病例,分別為22例本土個案及34例境外移入(10例為航班落地採檢陽性);另確診個案中無新增死亡。
-

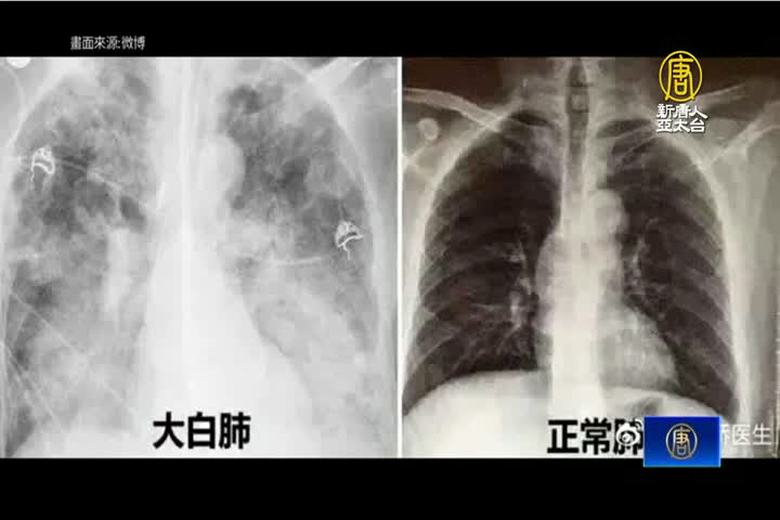
中共與天鬥清零失敗 陸網友轟「白肺心肌」
2023-01-03 16:38:54中共長達三年的清零封控失敗,現在疫情大爆發,出現「白肺」與「心肌炎」症狀的患者不斷蔓延至各個年齡層,有網友發文,家裡剛出生5天的新生兒,感染後遭醫院下病危通知書,右肺1/3出現白肺。由於中國本輪疫情中出現了大量「白肺」和「心肌炎」患者,中國網友更是創出了「白肺心肌」一詞,諷刺中共戰天鬥地的無效三年「清零」。目前,國際持續要求中共公布真實疫情數據,中國醫衛專家張文宏指出,過年期間,中國染疫比率可能高達80%,代表中國14億人口將有超過11億人染疫。
-

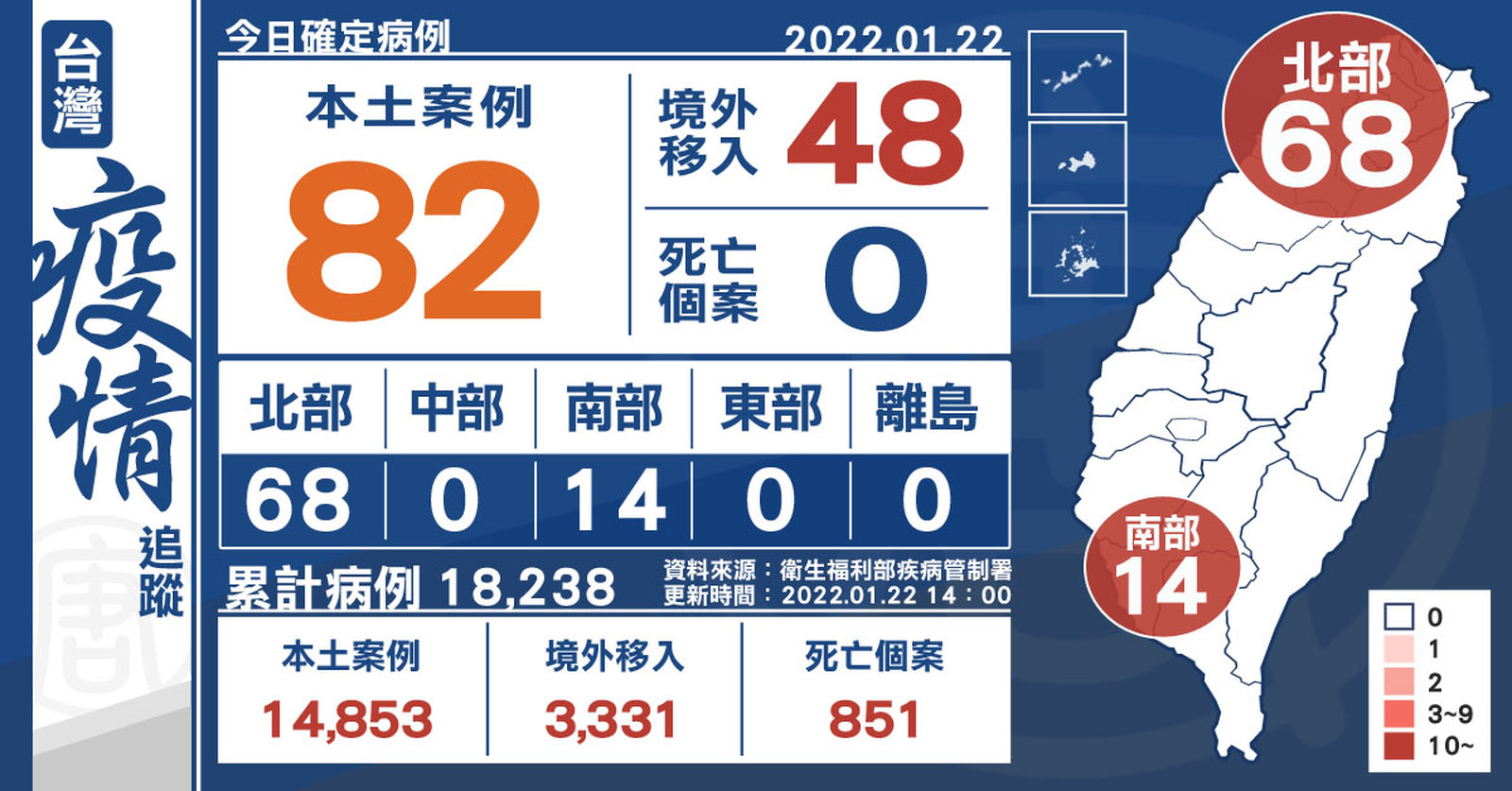
本土+82、境外+48 亞旭桃園廠群聚累計70人
2022-01-22 15:49:23今(22)日中央流行疫情指揮中心公布,國內新增130例COVID-19確定病例,分別為82例本土個案及48例境外移入;另確診個案中無新增死亡。
-

本土+15 桃園9例最多 境外移入+33 美國最多
2022-01-29 15:09:03今(29)日中央流行疫情指揮中心公布,國內新增15例本土個案及33例境外移入;另確診個案中無新增死亡。
-

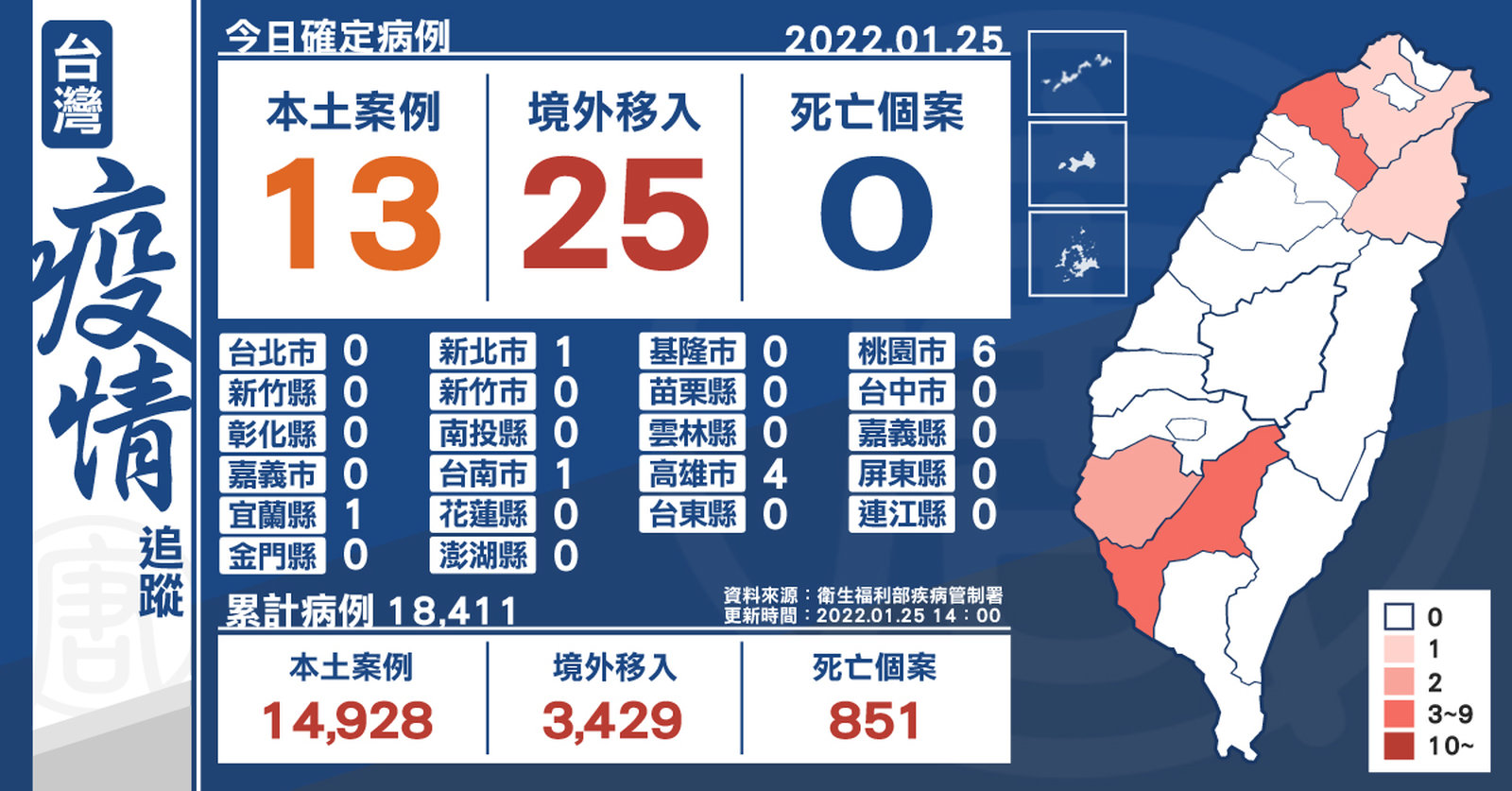
本土+13 境外移入+25 桃園增加3例不明感染源
2022-01-25 15:12:37今(1/25)中央流行疫情指揮中心宣布,新增13例本土、25例境外移入,死亡個案則未增加。新增本土個案為4例男性、9例女性,年齡介於未滿5歲至70多歲。
-

本土+15例 境外移入+36例 新年期間維持二級警戒標準
2022-01-24 15:27:42今(24)日中央流行疫情指揮中心公布,國內新增51例COVID-19確定病例,分別為15例本土個案及36例境外移入;另確診個案中無新增死亡。
-

+37例本土 11例陰轉陽 26例不明感染源 46例境外移入
2022-02-10 15:03:47今(10)日中央流行疫情指揮中心公布,國內新增83例COVID-19確定病例,分別為37例本土個案及46例境外移入,15例為航班落地採檢陽性;另確診個案中無新增死亡。
-

本土+14、死亡+1、境外51例 銀行員相關累計14人確診
2022-01-13 15:16:17今(13日)中央流行疫情指揮中心公布,新增本土14例、境外移入51例,另增1起死亡個案
-

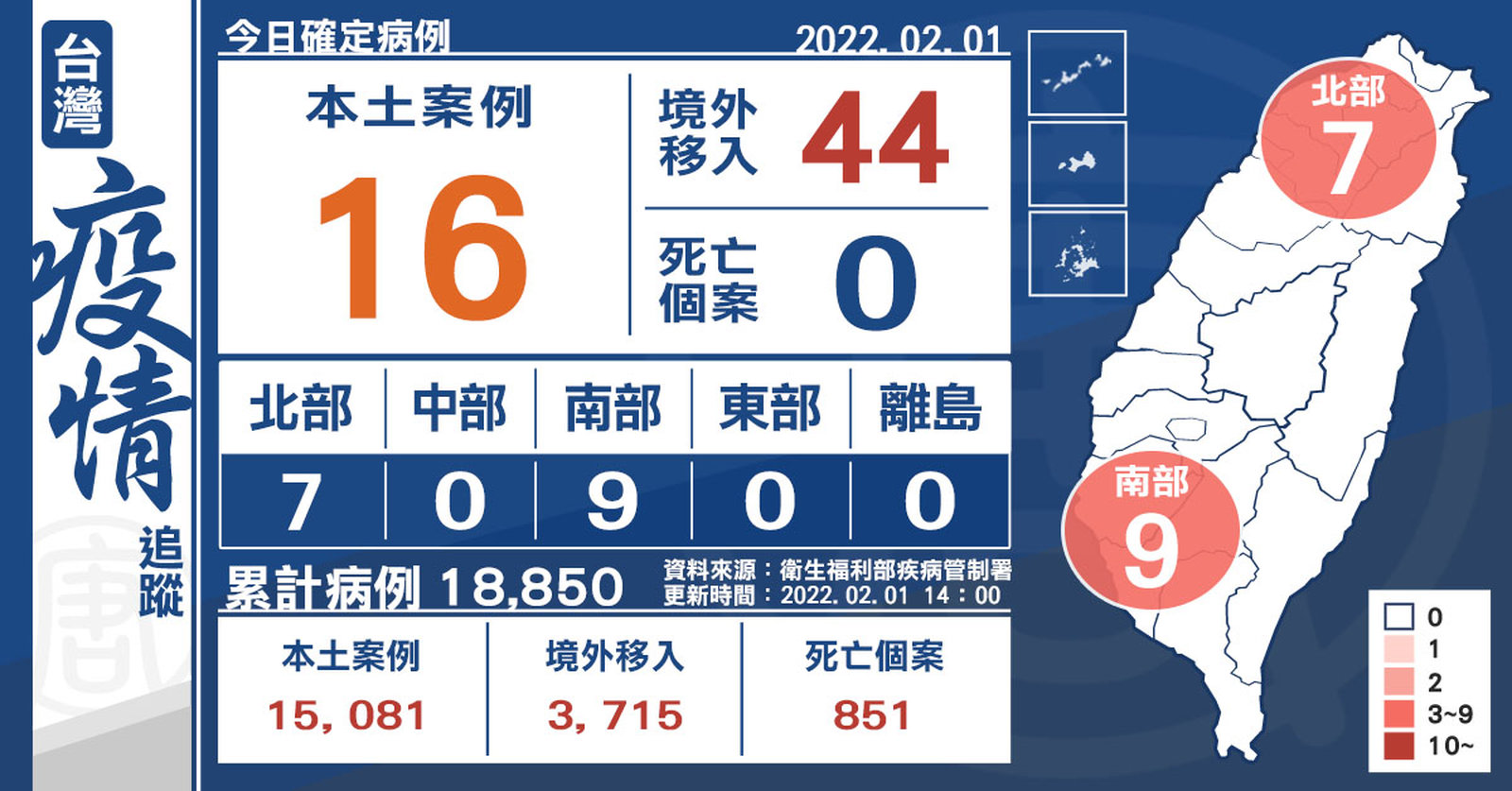
+16例本土 44例境外移入 7例落地採檢陽性
2022-02-01 15:05:48今(1)日中央流行疫情指揮中心公布,國內新增16例本土個案及44例境外移入,其中7例為航班落地採檢陽性;另確診個案中無新增死亡。
-

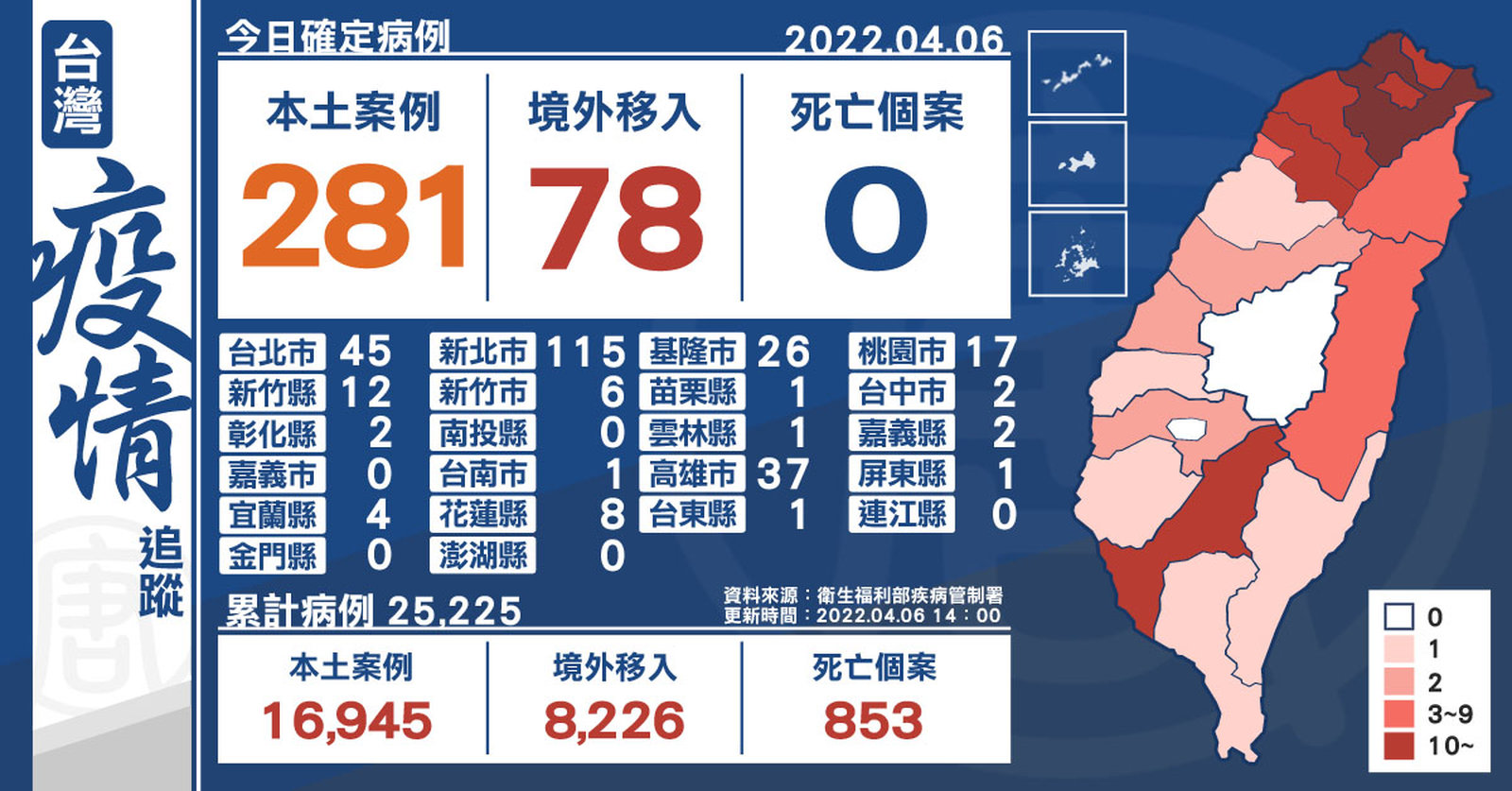
本土+281 全台17縣市確診 境外+78
2022-04-06 15:03:09中央流行疫情指揮中心今(6)日公布,國內新增359例COVID-19確定病例,分別為281例本土個案及78例境外移入,其中27例為航班落地採檢陽性;另確診個案無新增死亡。
-

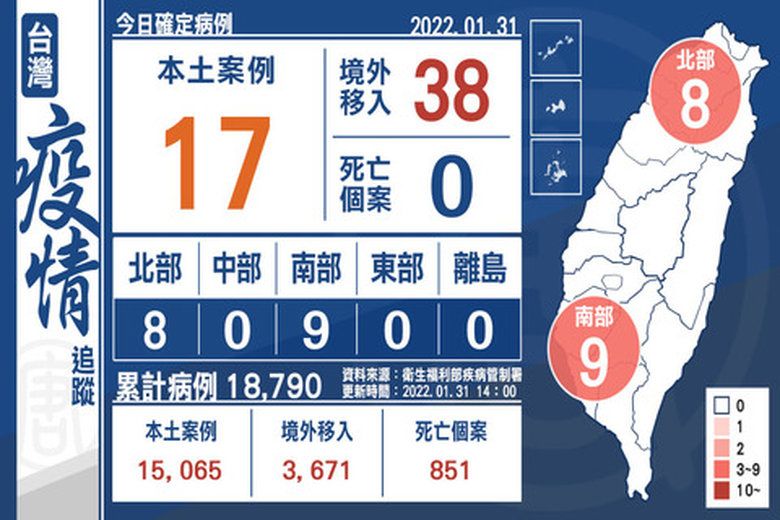
+17例本土 38例境外移入 美國最多
2022-01-31 16:33:40今(31)日中央流行疫情指揮中心公布,國內新增17例本土個案及38例境外移入(20例為航班落地採檢陽性);另確診個案中無新增死亡。
-

台本土+133 境外+142 雙北、桃園確診數多
2022-04-04 14:52:39中央流行疫情指揮中心今(4)日公布,國內新增275例COVID-19確定病例,分別為133例本土個案及142例境外移入,其中68例為航班落地採檢陽性;另確診個案無新增死亡。
-

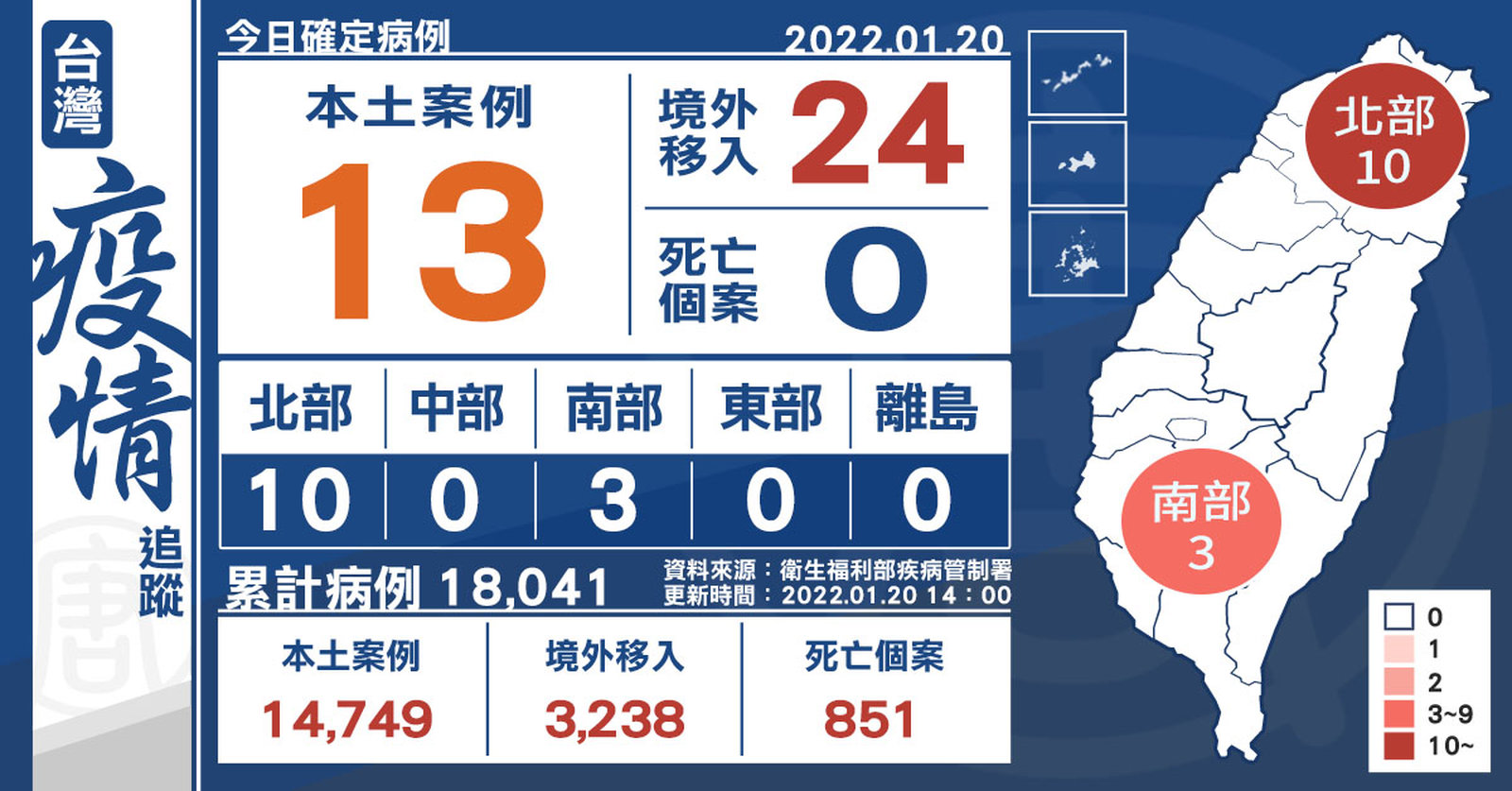
本土+13 境外+24 新確診一家三口與高雄港有關
2022-01-20 15:24:14今(20)日中央流行疫情指揮中心公布,國內新增37例COVID-19確定病例,分別為13例本土個案及24例境外移入;另確診個案中無新增死亡。
-

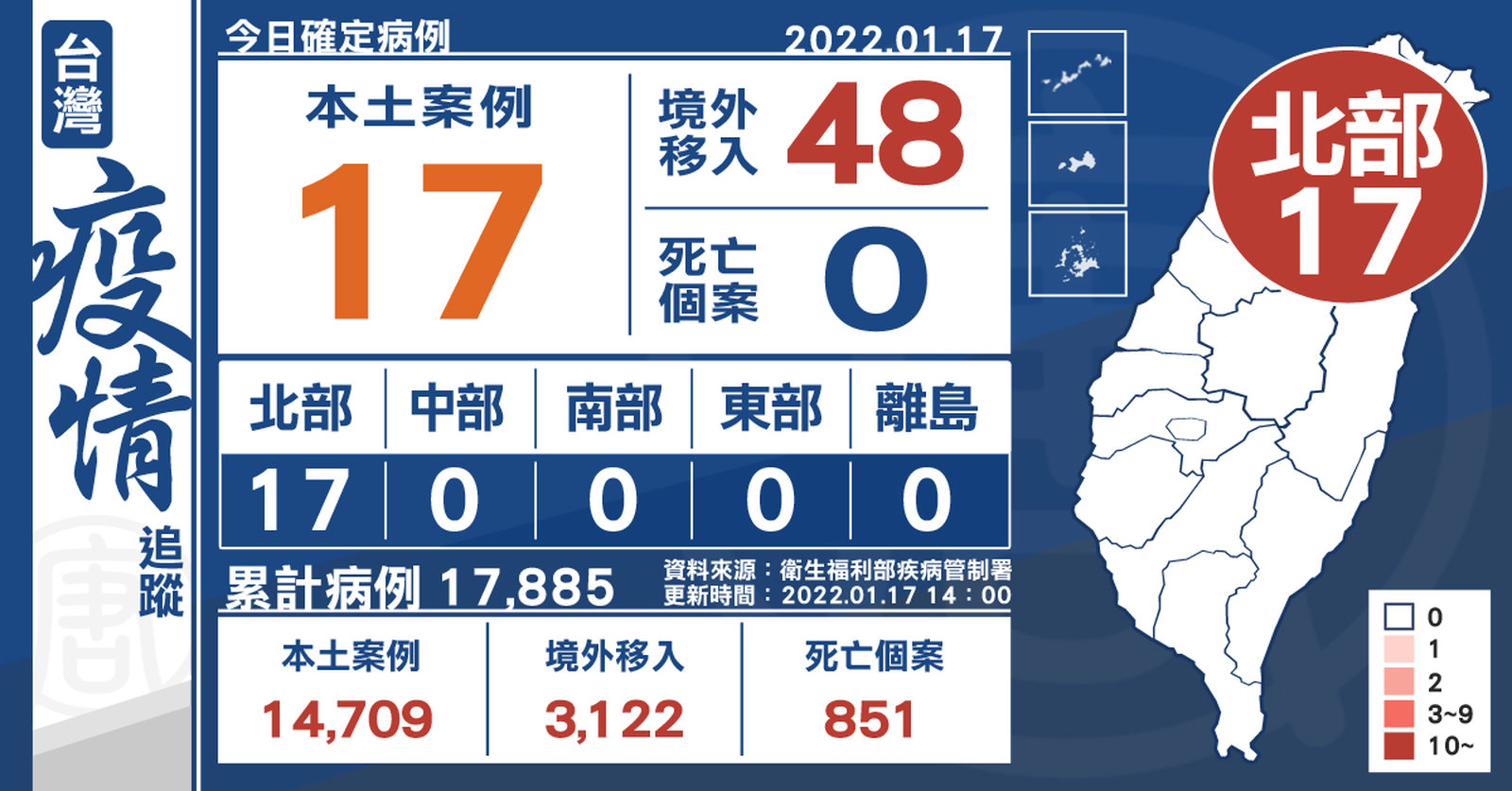
本土+17 西堤案已35例確診 境外+48 落地檢37居檢11
2022-01-19 15:01:53今(17)日中央流行疫情指揮中心公布,國內新增65例COVID-19確定病例,分別為17例本土個案及48例境外移入;另確診個案中無新增死亡。
-

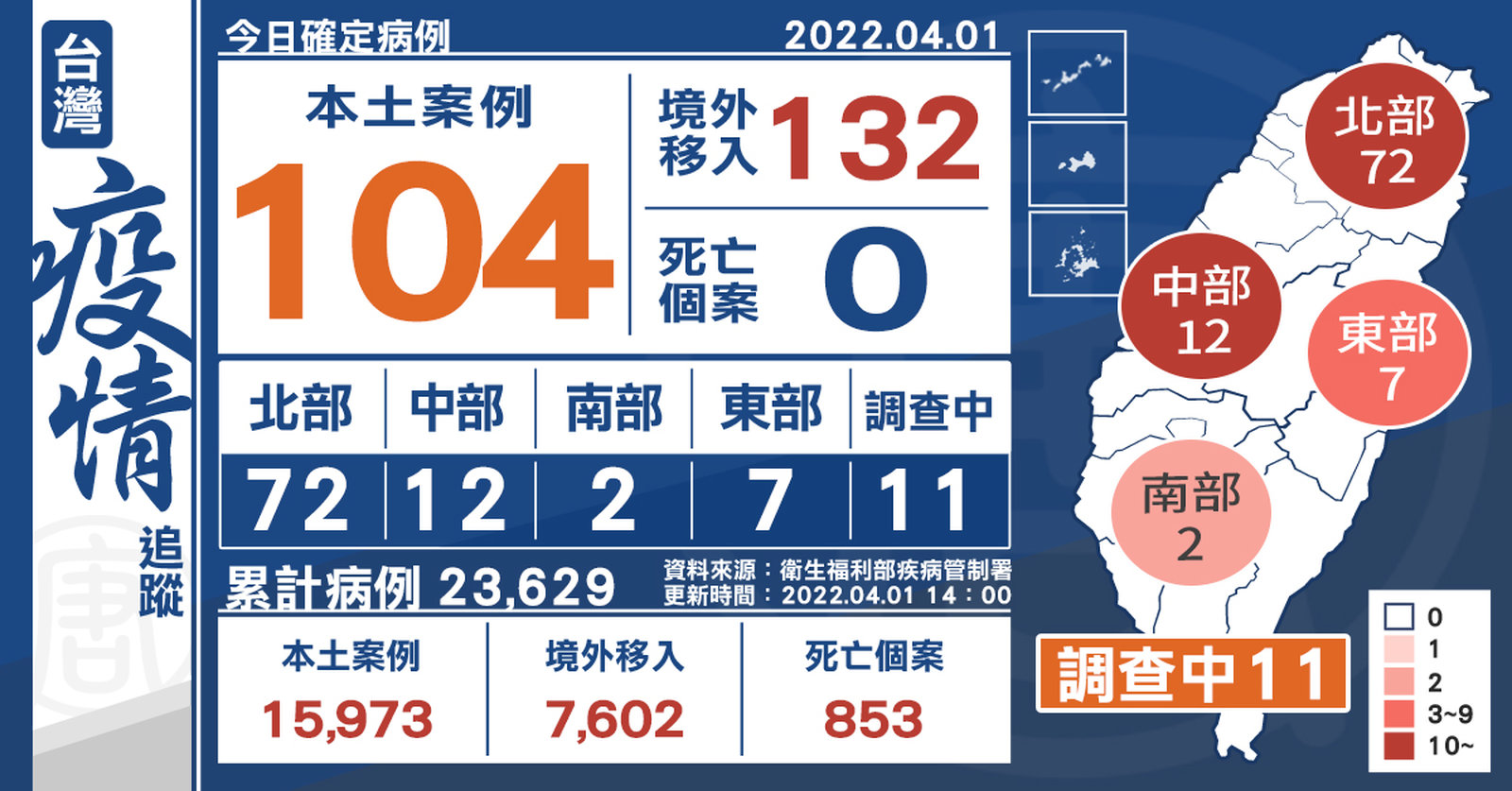
台本土+104 境外+132 桃園電商群聚新增22例
2022-04-01 14:45:34中央流行疫情指揮中心今(1)日公布,國內新增236例COVID-19確定病例,分別為104例本土個案及132例境外移入,其中75例為航班落地採檢陽性;另確診個案無新增死亡。