聯亞疫苗:準三期符WHO方向.若解盲失敗有備案
【新唐人亞太台 2021 年 06 月 03 日訊】台灣國產疫苗進度受關注。國民黨智庫國政基金會今天(3日)舉行座談,聯亞生技營運長彭文君應邀回應外界的關心與質疑,強調政府絕對沒有圖利廠商;他表示國產疫苗能應對多種變種病毒株,萬一解盲失敗,也有備案,同時在開發因應變種病毒疫苗、以及新一代疫苗。
聯亞生技營運長 彭文君:「6月可以解盲,6月底送EUA緊急授權,7月希望可以通過核准。」
台灣國產疫苗,高端、聯亞兩家,都在臨床試驗二期收尾階段,預計6月中將先後解盲,符合標準就申請台灣政府緊急授權。
聯亞生技營運長 彭文君:「萬一如果解盲失敗,我們實際上有其他備案,我們有其他疫苗在開發,我們有變種病毒疫苗也在開發,也會有新一代,我們目前測試效果,事實上比第一代更好。這跟國家現在簽約沒直接關係。」
外界質疑,沒做第三期就申請授權。聯亞生技營運長彭文君3日在國民黨智庫座談解釋,第二期原先規劃比照國外,做幾百人就趕快結束,進入三期試驗;但配合政府專家會議的共識,改採大規模二期做到3850人規模,形同「準三期」試驗;世衛組織會議也達成共識,透過「疫苗中和性抗體力價」、與「COP保護力關聯測試」,來縮短疫苗上路的時間。他說,台灣政府與法規很嚴格,絕對沒放水,每周開會檢討。
聯亞生技營運長 彭文君:「(政府先)簽約絕對不是說就買單,也不是啊,若後面EUA緊急授權沒通過,實際上這正式採購就沒有了,所以這怎麼會有圖利之說,這是不可能的。」「絕對沒有放水這件事,非常嚴格的,我說的(政府法規面)支持是說,是採取滾動式審查,聯亞每天有資料出來就送出去,他們(政府人員)都半夜在看資料,我們也半夜在整理資料,每天是這樣做的。」
彭文君說,台灣的感染人數跟國外相比太懸殊,不具備條件在台灣當地做三期試驗。不過,媒體報導,國產疫苗先爭取台灣緊急授權之外,仍打算做三期試驗,聯亞打算向印度申請上萬人試驗;高端打算在歐洲荷蘭展開,力拚半年內取得歐盟藥品管理局(EMA)認證。
中華民國醫師公會全聯會副秘書長 羅浚晅醫師(2021.06.02):「不是這樣就不做三期的臨床試驗,而是兩個部分要一起來,這樣子才能把握一個足夠的時間,製造出足夠的疫苗。」
聯亞生技營運長 彭文君:「我們的策略未來會是可以在,不管你是打別家的疫苗,或是打個原來的兩針、或原來的疫苗打下去,後面再補一針,可能就可以做到對抗變種病毒。」
彭文君指出,聯亞疫苗,對於變種英國株、南非株都有不錯效果;希望今年底生產1億劑,明年量產5億到8億劑,輸出國外,因為世界上還有五、六十億人無疫苗可打。
新唐人亞太電視 黃亮戩 張東旭 台灣台北報導。
相關新聞
-

神韻2023台灣首站苗栗爆滿 金曲歌王.政要盛讚
2023-02-26 09:25:51美國神韻世界藝術團,24日起在台灣展開5大城市的巡迴演出,第一場今天(24日)在苗北藝文中心登場,吸引台灣各界政要、藝文界人士觀看。節目精采完美的呈現,觀眾們熱情鼓掌,謝幕兩次。
-

中共海警圍攻襲擊菲律賓船隻 美日台同聲譴責
2024-06-20 19:40:26中共對菲律賓船隻的襲擊引起周邊國家關注。中華民國外交部表示,台灣反對任何以武力片面改變現狀的企圖,以及在南海的灰區行動與軍事脅迫。美國國務卿布林肯也與菲律賓外長通話,譴責中共破壞區域和平穩定,並重申美國根據《共同防禦條約》對菲律賓的堅定承諾。此外,日本自衛隊統合幕僚長吉田圭秀,也與菲律賓參謀總長進行視訊通話,雙方都對事態發展表示擔憂。吉田圭秀強調,日本自衛隊始終站在菲律賓這邊,並將深化與菲律賓及理念相近國家的合作。
-

颱風「格美」襲擊中國多地 中共壓熱搜
2024-07-27 19:32:54強颱風「凱米」中國稱「格美」橫過台灣,並在7月25日晚登陸中國福建,26日移向浙江、江西等地,並將影響中國10多個省。各地網民展示颱風造成的慘況,但中共淡化消息。來看詳情:
-

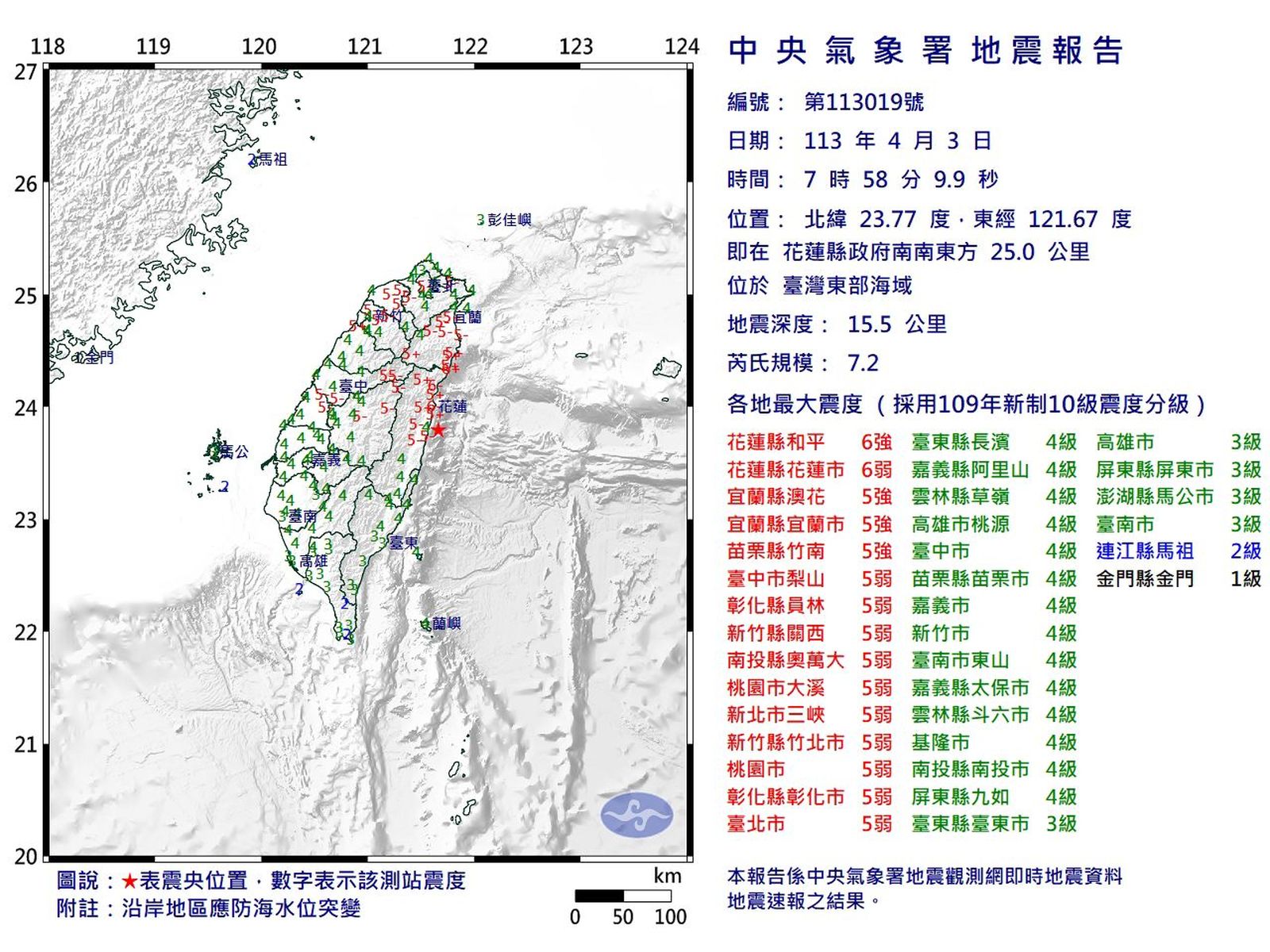
花蓮芮氏規模7.2強震全台有感 高鐵、捷運暫停行駛
2024-04-03 11:18:06今天上午7點58分,花蓮地區發生芮氏規模7.2地震,震央位置約在花蓮縣政府南南東方25.0公里,位於臺灣東部海域,地震深度15.5公里。
-

斷交台灣後中共1隻都沒買 宏國白蝦出口少25%
2024-04-08 07:22:43台灣與宏都拉斯在去年3月斷交,轉與中共建交後,由於兩國自由貿易協定(FTA)尚未談妥,加上開價比台灣低5成,蝦農賣給中國意願不高,加上台宏外交關係生變後,出口到台灣的白蝦必須課徵20%的關稅,墨西哥對宏國蝦祭出禁令,宏都拉斯國家水產養殖者協會(Andah)最新統計顯示,2024年第一季白蝦出口量為1697.6萬磅,低於去年前3月的2282.5萬磅,出口量下滑25.82%。
-

台裔女孩張芳瑜 贏得美國亞洲小姐后冠
2023-11-20 19:52:39歡迎回來。2023年美國亞洲小姐(Miss Asia USA)決賽,就讀美國史丹佛大學的張芳瑜(Tiffany Chang),奪得第35屆美國亞洲小姐后冠。20歲的張芳瑜,代表台灣參賽,身上披的彩帶寫著Taiwan,穿著類似古代漢服的服裝,她是台灣移民第二代,曾獲選2022台美小姐,這次在亞洲小姐比賽中榮獲四個獎項。現場有上百名台僑,手舉中華民國國旗和標語為她加油。張芳瑜以科技女性投身選美,她感到有特殊意義,希望透過這次的勝利能夠突顯台灣的地位。
-

前中軍醫來台曝罪行 朝野立委推反活摘器官法
2024-07-16 07:33:26歡迎回來,90年代曾在中共軍醫院參與活摘器官的醫生鄭治,今天出席台灣立法院記者會,曝光中共罪行;朝野立委強調,會繼續在台灣推動制定「打擊及防制活摘器官法」,美國、日本議員也錄影片表達支持,共建法律防火牆。
-

杭州亞運台灣19金20銀28銅 金牌數追平隊史紀錄
2023-10-08 15:49:00杭州亞運今天(8日)進入最後一天的賽程,台灣空手道女將谷筱霜在女子50公斤級的金牌戰中,擊敗哈薩克選手然格貝爾拜(Moldir Zhangbyrbay),為中華隊拿下今年的第19面金牌。
-

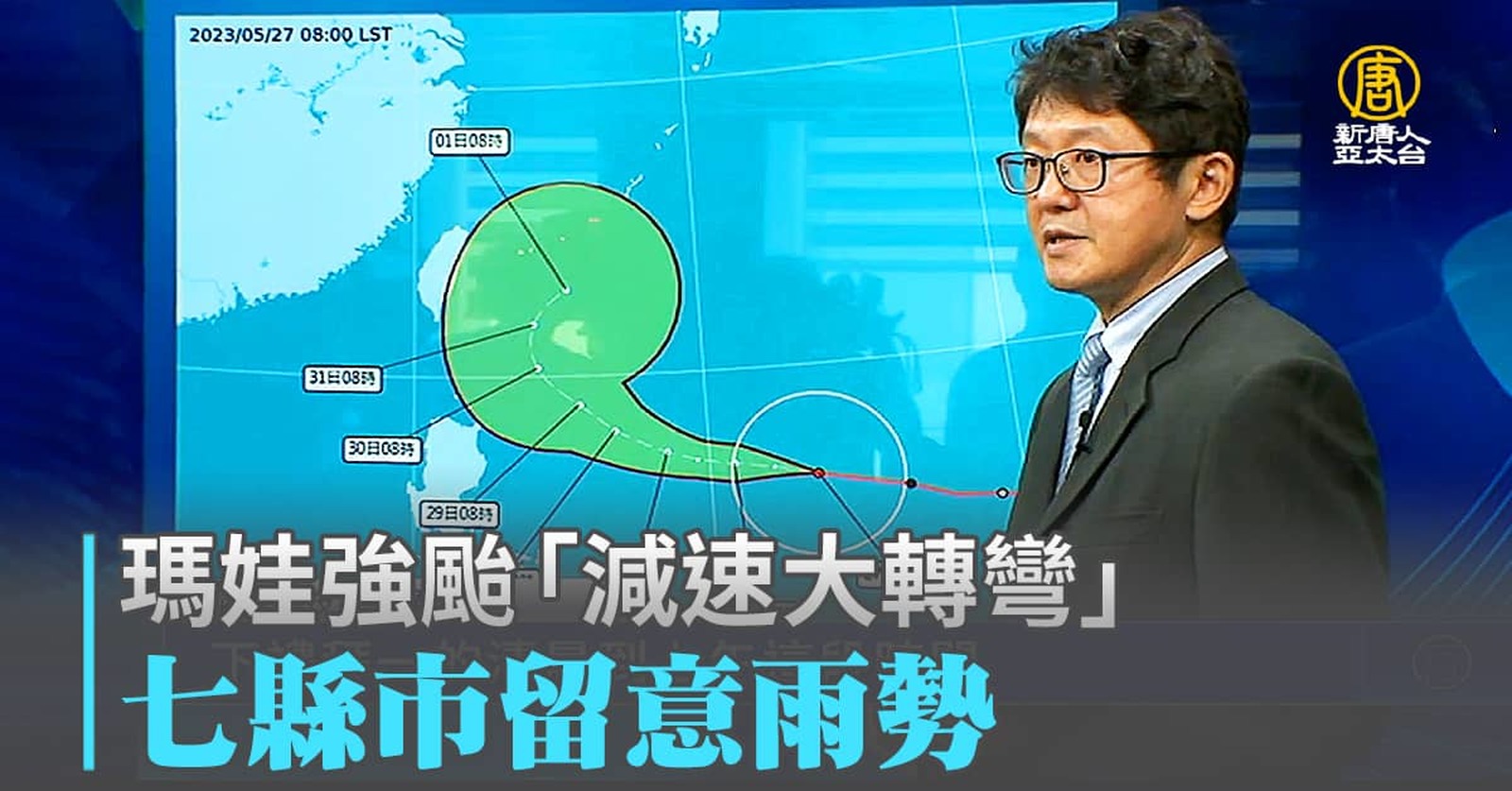
瑪娃強颱「減速大轉彎」 七縣市留意雨勢
2023-05-27 19:23:59強烈颱風「瑪娃」持續穩定朝西前進,台灣中央氣象局預計週一(5月29日)清晨到上午,就會發布海上颱風警報,但由於週一會開始北轉,發布陸警的機率低,不過,從下週一到下星期四,北北基宜與花東、恆春半島的民眾,都要留意雨勢。
-

英外相訪中 英國會稱中華民國台灣是獨立國家
2023-08-30 12:54:39再來看到,英國外交大臣柯維立今天(30日)訪問中國,英國國會外交事務委員會今天發布報告,內容中首度直接稱台灣是一個獨立國家,名字就叫做中華民國。
-

義專家:台對全部人重要 半導體給我們上一課
2023-09-12 13:02:39地緣政治影響半導體業程度加劇,各國爭相邀請台積電到當地投資,義大利一位兩岸專家在電視節目中,談論台灣晶片的無可取代性,以及台灣對全世界的重要性,義大利也希望台灣轉移部份半導體生產。
-

不能沒台灣! 蘇姿丰:半導體生態系令人驚嘆
2023-07-20 19:37:06今天下午,超微半導體執行長蘇姿丰,出席在陽明交大舉行的頒授名譽博士學位典禮。蘇姿丰表示,這週的訪問行程,讓她感受到,台灣確實是全球半導體生態系的中心。
-

空中保衛台灣 台兩位女飛官登英國媒體
2023-06-19 13:23:34中共擾台行為層出不窮,近來頻頻發生共軍飛機逾越海峽中線的狀況,國軍對此密切監控並派機攔截,其中女性戰機飛行員郭文靜上尉和謝蕓梃少校受到了外媒注意。
-

神韻完美至極 醫院院長敬佩藝術總監
2023-02-27 20:38:43新竹惠民醫院院長謝其文,25日晚間,在苗北藝文中心欣賞了美國神韻世界藝術團的第三場演出,他說,神韻演出完美至極,感佩藝術總監,讓台灣觀眾能夠欣賞到國際頂級藝術饗宴。
-

南韓跌出全球10大經濟體 人均GDP也輸台灣
2023-07-13 17:16:19南韓央行週三(12日)公布數據,顯示2022年名目GDP為1.67兆美元,排名全球第13名,南韓時隔3年,再次跌出世界前10大經濟體地位,分析指出主因為美元走強、韓元貶值,出口表現不佳也是原因之一,IMF推估今年韓國經濟成長率為1.5%,要重回全球前10大可能性也不高。另外根據數據,2022 GDP台灣排名第21名,亞洲四小龍中僅次於南韓,不過如果以人均GDP計算,台灣2022年人均GDP達到35510美元,南韓為33590美元,這是台灣自2003年以來第一次超越南韓。
-

盧沙野稱烏克蘭等前蘇聯非國家 引中東歐大使關切
2023-04-22 20:48:26帶您看到,中共駐法大使盧沙野的戰狼式發言,再度惹怒國際。21日盧沙野接受法國媒體訪問時,聲稱前蘇聯國家,包括烏克蘭等,都沒有正式的國際地位,引發議論,中東歐國家的大使集體質疑,難道對盧沙野來說,立陶宛、愛沙尼亞都不是國家?
-

《演員夢》南台灣上映 觀眾:重拾正念讓人生變彩色
2023-06-08 18:32:11新世紀影視推出電影《演員夢》,獲國際各大電影節16個獎項,5月起在台灣北中南六城市上映。國會議員觀影後讚許,這部片讓人生重拾正念力量;前地檢署官員感受,《演員夢》讓人生從黑白變彩色。6月中旬還將在新竹、宜蘭上映。
-

陳建仁授旗第2梯土國救難隊 台援款200萬美元
2023-02-08 10:28:31台灣首批搜救隊6日晚間搭機前往土耳其救災,第二批搜救人員也在昨晚出發,除了90名來自消防署、台北市、台中市、屏東縣的搜救隊員,還有2隻搜救犬及6.4公噸儀器設備,包括最先進的生命偵測器,行政院長陳建仁特別到場授旗,他說,相信隊員一定能達成任務,讓世界看到Taiwan is helping。另外,中華民國外交部也宣布捐贈土耳其政府的賑災援款,提高至200萬美元,以進一步幫助土耳其政府安置災民。外交部也公布土耳其賑災捐款專戶。
-

【座談影音】11/24(日)面對美國新政局 台灣應如何趨吉避凶?
2024-11-26 18:59:29川普勝選對中共國,會有何等的衝擊,而中共又會如何出招,對台的文攻武嚇?台灣應如何趨吉避凶?我們邀請明居正、矢板明夫、宋國誠以及謝金河四位名家,指點迷津!
-

立陶宛下週大選 台灣代表處命名議題再受矚
2024-05-08 12:58:18台灣與歐洲友好關係升溫,立陶宛即將舉行總統大選,不過正在競選連任的現任總統瑙塞達卻說,他認為應該要更改台灣駐立代表處的名稱。這番言論引起其他候選人的批評,包括現任總理席莫尼特。她強調,如果強迫台灣改名,只會讓立陶宛信譽盡失。